Cercetătorii de la Universitatea din Pennsylvania (Penn) au creat un dispozitiv, realizat prin microinginerie, care găzduieşte un model viu şi vascularizat de cancer pulmonar uman, o „tumoră pe cip”, şi au descoperit că un medicament utilizat în tratamentul diabetului zaharat de tip 2 poate îmbunătăţi eficienţa imunoterapiei CAR-T, permiţând celulelor imunitare să pătrundă mai uşor în ţesutul tumoral şi să-l atace mai eficient.
Terapia cu celule T modificate genetic (CAR-T, de la Receptor de Antigen Chimeric / Chimeric Antigen Receptor T cells) a revoluţionat tratamentul unor forme de cancer hematologic (al sângelui), precum leucemiile şi limfoamele. Metoda constă în prelevarea limfocitelor T de la pacient, reprogramarea lor pentru a recunoaşte antigenele tumorale şi reintroducerea acestora în organism.
Cu toate acestea, succesul a fost limitat în cazul tumorilor solide, care reprezintă peste 90% dintre cancere. Mediul microtumoral, un sistem complex şi ostil, cu vase de sânge anormale sau deteriorate şi semnale biochimice care ascund celulele maligne, funcţionează ca un adevărat zid de protecţie împotriva atacului sistemului imunitar.
Echipa de la Penn, condusă de profesorul Dan Dongeun Huh, de la Facultatea de Inginerie şi Ştiinţe Aplicate, a dezvoltat un model inovator de „tumoră pe cip” pentru a studia direct aceste interacţiuni.
Dispozitivul transparent oferă o fereastră asupra „câmpului de luptă” dintre sistemul imunitar şi cancer, permiţând cercetătorilor să observe în timp real cum celulele CAR-T se deplasează prin ţesutul tumoral, atacă celulele canceroase sau, uneori, eşuează.

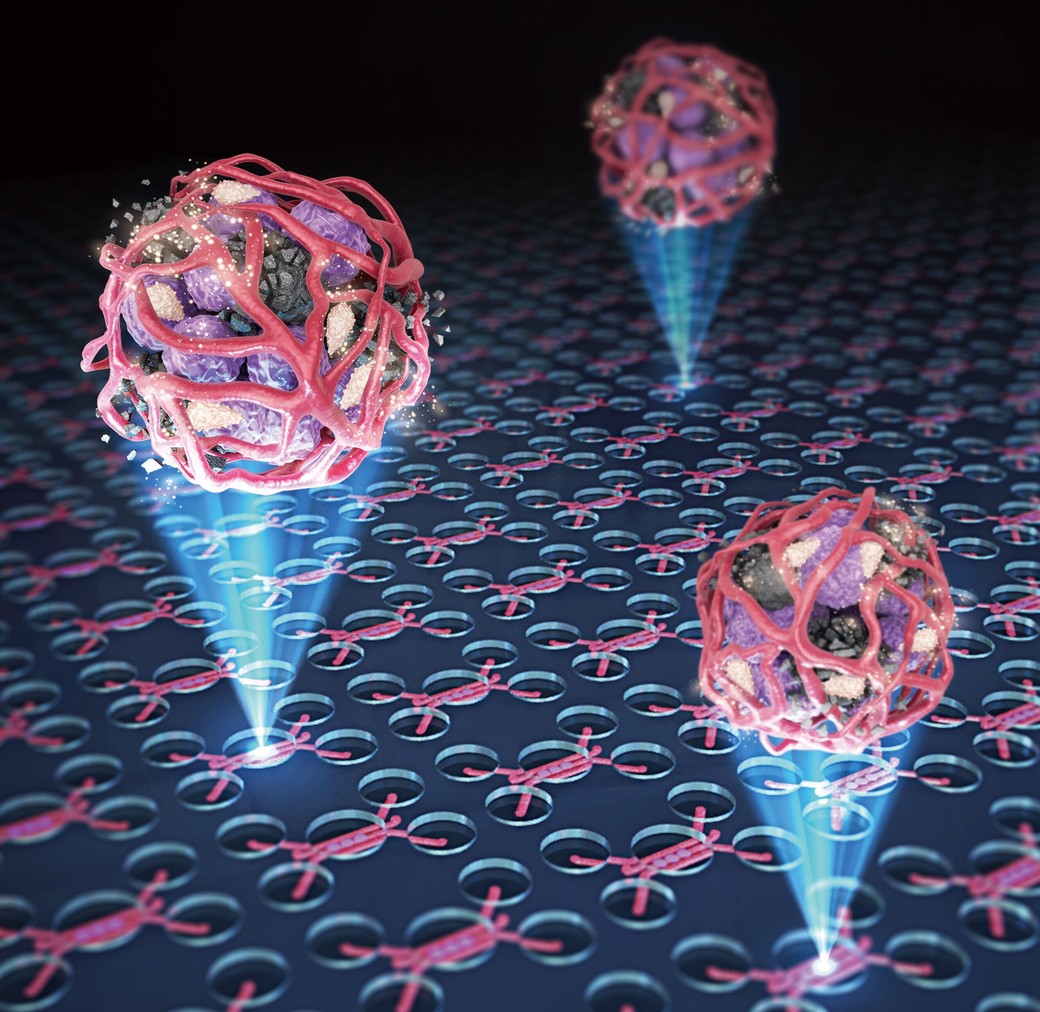
Cercetătorii de la Universitatea din Pennsylvania au dezvoltat un dispozitiv transparent, creat prin microinginerie, care găzduieşte un model viu şi vascularizat de cancer pulmonar uman - o „tumoră pe cip” - şi au demonstrat că medicamentul pentru diabet vildagliptin ajută un număr mai mare de celule CAR-T să pătrundă prin mecanismele de apărare ale tumorii şi să o atace eficient. Credit: Dan Huh, Penn, 23 octombrie 2025
Prin integrarea tehnologiilor multiomice, care combină date genetice, proteomice şi metabolice, cu instrumente de bioinformatică avansată, cercetătorii au identificat o enzimă, DPP4, produsă atât de fibroblaste, cât şi de celulele T, ca fiind responsabilă pentru degradarea rapidă a semnalelor chimice care atrag celulele imunitare către tumoră.
Întrucât enzima şi inhibitorii acesteia au fost bine documentaţi în studiile despre diabet, echipa a testat medicamentul vildagliptin, un inhibitor DPP4 utilizat clinic pentru diabetul zaharat de tip 2.
Rezultatele au arătat că medicamentul a menţinut mai mult timp integritatea acestor semnale, permiţând unui număr mai mare de celule CAR-T să ajungă la ţesutul tumoral şi să se infiltreze eficient în acesta.
Într-un experiment observat direct prin microscopie fluorescentă, cercetătorii au urmărit cum o singură celulă T traversează peretele unui vas sanguin, migrează prin ţesut şi atacă un grup de celule canceroase. Până acum, astfel de procese puteau fi doar deduse din studii preclinice pe animale.
Studiul, publicat în luna octombrie, în revista Nature Biotechnology, deschide drumul către evaluarea rapidă şi sigură a unor noi variante de celule CAR-T şi sugerează că modelele de tip organ-pe-cip pot reduce semnificativ utilizarea modelelor animale în cercetarea biomedicală.
Potrivit autorilor, faptul că acest model reproduce fidel procesele fiziologice umane permite obţinerea de date preclinice relevante, care pot accelera dezvoltarea unor imunoterapii mai eficiente şi mai sigure pentru pacienţii cu cancer.
Credit imagine articol: Haijiao Liu, Universitatea Penn, 23 octombrie 2025.