Un mecanism-cheie al regenerării nervoase deficitare în diabet sugerează o nouă ţintă terapeutică. Identificarea noii căi biologice indică o nouă ţintă de tratament, care ar putea ajuta la repararea leziunilor nervoase cauzate de diabet.
Studii recente arată că afectarea nervilor la persoanele cu diabet, cunoscută ca neuropatie diabetică, nu este doar o consecinţă inevitabilă a bolii, ci ar putea fi influenţată prin intervenţii care reactivează capacitatea naturală de refacere a fibrelor nervoase.
O echipă de cercetători a identificat acum un mecanism central care blochează regenerarea şi a testat o abordare experimentală ce restabileşte acest proces în modele preclinice, oferind indicii pentru viitoare terapii.
Leziunile nervoase reprezintă una dintre cele mai frecvente şi împovărătoare complicaţii ale diabetului, milioane de pacienţi din întreaga lume confruntându-se cu durere, amorţeală şi limitarea mişcărilor.
Problema majoră este aceea că fibrele nervoase distruse se regenerează insuficient, iar cauzele biologice ale acestei incapacităţi au rămas până acum neclare.
Un grup de cercetare condus de prof. dr. Dietmar Fischer, profesor de farmacologie la Facultatea de Medicină a Universităţii din Köln şi director al Centrului de Farmacologie din cadrul Spitalului Universitar Köln, a identificat un mecanism care explică de ce regenerarea nervoasă este inhibată în diabet.
Rezultatele au fost publicate miercuri, în revista Science Translational Medicine.
Folosind modele murine de diabet zaharat tip 1 şi tip 2, cercetătorii au observat o acumulare crescută a proteinei p35 în celulele nervoase. Această proteină activează enzima CDK5 - o kinază dependentă de ciclina 5-, declanşând o cascadă de semnalizare care blochează recreşterea fibrelor nervoase după leziune.
Consecinţa acestui mecanism este restrângerea semnificativă a capacităţii naturale de regenerare a nervilor, observate în acest caz la animalele cu diabet. Echipa a intervenit ţintit pe această cale de semnalizare, fie prin metode genetice, fie prin utilizarea unor blocuri proteice mici nou dezvoltate, de tip peptide, administrate sistemic.
Prin inhibarea hiperactivităţii CDK5 mediate de p35, blocajul regenerării terminaţiilor nervoase a fost îndepărtat. În aceste modele preclinice, fibrele nervoase au început să crească din nou cu o rată comparabilă cu cea observată la animalele sănătoase, iar acest lucru s-a tradus prin îmbunătăţiri motorii şi senzoriale semnificative.
„Pentru prima dată, rezultatele noastre arată că vindecarea nervilor în diabet poate fi readusă la un nivel similar cu cel al animalelor sănătoase dacă activarea excesivă a acestei căi de semnalizare este inhibată. Chiar şi când neuropatia diabetică este deja instalată, apare o îmbunătăţire a regenerării”, a declarat prof. dr. Fischer, citat într-un comunicat.
O peptidă dezvoltată şi brevetată de grupul său pare deosebit de promiţătoare, întrucât vizează direct cauza biologică identificată şi, în principiu, ar putea fi dezvoltată într-un medicament.
Un alt aspect important este faptul că slăbirea regenerării nervoase indusă de diabet apare chiar înainte de instalarea neuropatiei diabetice, complicaţie care afectează aproape jumătate dintre pacienţi.
Cercetătorii investighează în continuare dacă mecanismul p35–CDK5 contribuie direct la declanşarea bolii sau dacă riscul poate fi redus prin noile opţiuni terapeutice propuse.
În ansamblu, studiul deschide perspective noi pentru tratamentul şi, posibil, prevenţia leziunilor nervoase din diabet, cunoscute ca neuropatie diabetică, una dintre cele mai răspândite şi încă incurabile complicaţii cronice ale acestei afecţiuni.
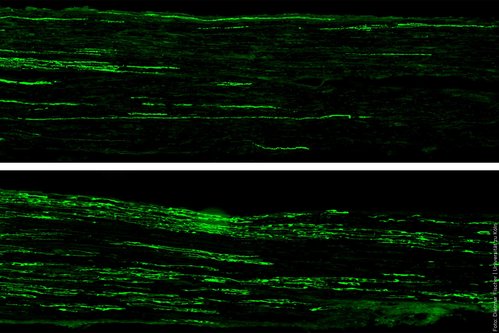
Secţiuni longitudinale în doi nervi lezaţi, cu fibre nervoase în regenerare. Ambele probe provin de la animale cu diabet; în imaginea de jos, animalul a fost tratat cu o peptidă. Regenerarea este vizibilă în fibrele nervoase colorate în verde. Credit: Dietmar Fischer, Universitatea din Köln, 26 noiembrie 2025